Fotosíntesis en bacterias verdes
Un equipo internacional ha determinado la estructura de la molécula de clorofila de las bacterias verdes. Este resultado quizás permita algún día recrear una fotosíntesis artificial eficiente.

|
|
|
Estos científicos han descubierto que las moléculas de clorofila de las bacterias verdes son muy eficientes captando energía luminosa. La razón parece ser la orientación de las propias moléculas.
Las bacterias verdes son un grupo de organismos que viven generalmente en ambientes pobres en luz, como las regiones oscuras de fuentes hidrotermales a 100 m de profundidad del mar Negro. Estas bacterias contiene estructuras denominadas clorosomas que contienen unas 250.000 moléculas de clorofila.
Donald Bryant, de Penn State, recuerda que la habilidad de capturar la energía luminosa y suministrarla rápidamente en donde se necesite es esencial para estas bacterias, algunas de las cuales sólo ven unos pocos fotones por molécula de clorofila al día.
Los clorosomas de estas bacterias son difíciles de estudiar y han sido la última clase de complejos captadores de luz cuya estructura ha sido caracterizada. Saber la estructura de las proteínas (o en su tiempo la del ADN) no es tampoco sencillo. Para esta tarea se emplea normalmente la cristalografía de rayos X. Aunque un paso previo es conseguir que la molécula a estudiar cristalice de tal modo que muchas moléculas se dispongan de manera ordenada en una red cristalina. Por tanto, esta técnica sólo funciona si las moléculas a estudiar son uniformes en tamaño, forma y estructura.
Cada clorosoma de las bacterias verdes tiene una organización única y por tanto la técnica de cristalografía de rayos X no puede ser empleada para caracterizar su estructura interna.
Para solucionar este escollo los investigadores se valieron de varias técnicas. Una de ellas consistió en crear bacterias genéticamente modificadas que tuvieran una estructura más homogénea. También emplearon la microscopía electrónica y resonancia magnética nuclear. Todo esto les permitió saber incluso la estructura de los componentes de los clorosomas y tener un modelo completo de los mismos.
|
|
|
La ingeniería genética que practicaron es interesante porque para la creación del mutante tuvieron que desactivar tres genes que se adquirieron recientemente desde el punto de vista evolutivo. Los investigadores sospechaban que precisamente estos genes son los que proporcionan a las bacterias su mayor capacidad de captar la energía luminosa, por lo que esta ingeniería genética era como ir hacia atrás en el tiempo.
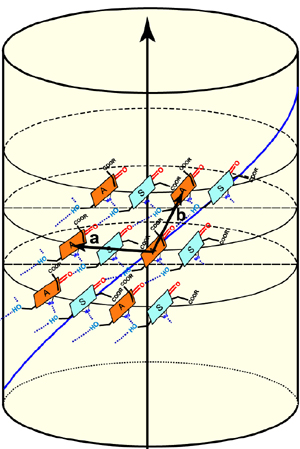
Para poder tomar las imágenes de microscopía electrónica hubo que enfriar las muestras hasta llegar a temperaturas criogénicas. Así pudieron ver que las moléculas de clorofila que hay dentro de los clorosomas tienen forma de nanotubo a la manera de muñecas rusas, con un tubo concéntrico dentro de otro. Las bacterias mutantes sólo contenían un conjunto de estos tubos mientras que las normales contenían varios, cada uno dispuesto en un patrón único.
Finalmente la resonancia magnética nuclear (RMN) reveló que las moléculas de clorofila venían dadas en forma de dímeros (parejas de dos moléculas idénticas) con sus colas hidrófobas unidas. Descubrieron además que las moléculas de clorofila de estos clorosomas se disponen en forma de hélice (de manera similar al ADN). En las bacterias mutantes estas moléculas se disponen en un ángulo de 90 grados en relación al eje del nanotubo siendo este ángulo menor en las bacterias naturales.
Lo importante parecer ser precisamente la orientación de las moléculas de clorofila, pues les permite recoger mayor energía luminosa. Todo esto fue posible a la capacidad de la RMN de situar espacialmente y con precisión los núcleos atómicos.
Parece contraintuitivo que las bacterias verdes hayan evolucionado para captar más energía solar desordenando las estructuras del clorosoma. Según Bryant la gente podría pensar que una estructura más ordenada funcionaría mejor, pero en este caso claramente no es verdad. Si todas las moléculas de clorofila fueran idénticas y estuvieran dispuestas de manera perfecta dentro del clorosoma, la energía de un fotón incidente, una vez absorbida, estaría dando vueltas por el sistema demasiado tiempo. En la versión natural la movilidad de esta energía se restringe y la energía de un fotón individual visita un número pequeño de moléculas. De este modo la capacidad de obtener energía allí donde se necesita se incrementa. La clave está en la velocidad. Los microorganismos tienen sólo un par de nanosegundos para utilizar en algún lugar la energía captada antes de que ésta se pierda. Y este problema de la velocidad puede ser grave para microorganismos como estas bacterias, que viven en lugares con poca luz, y que sólo reciben unos pocos fotones diarios por molécula de clorofila.
Bryant dice que este resultado quizás sea útil un día si se consigue desarrollar un sistema de fotosíntesis artificial que produzca electricidad a partir de la energía solar. La idea sería crear estructuras específicas con moléculas de clorofila o análogas en disolución acuosa para así optimizar la capacidad de absorber energía luminosa.
Una planta de cultivo normal sólo transforma en azúcares un porcentaje muy pequeño de la energía solar recibida, de ahí que, a priori, el uso de biocombustibles no sea tan buena idea como parece en una primera aproximación. Puede que sea mejor utilizar otro tipo de seres fotosintéticos. Recientemente se han producido, por ejemplo, avances con algas unicelulares en este sentido. Quizás este hallazgo también pueda ser utilizado para la producción de biocombustibles eficientes a través de una ingeniería genética que permita crear organismos más apropiados para su producción.
Fuentes y referencias:
Nota de prensa.
Artículo original (abierto).
Comentarios
Sin comentarios aún.
RSS feed for comments on this post.
Lo sentimos, esta noticia está ya cerrada a comentarios.