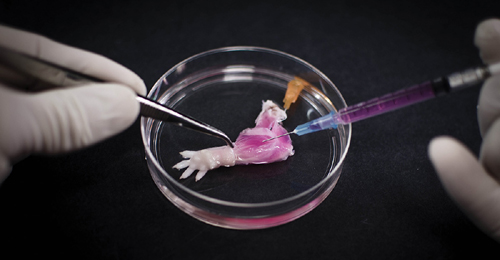
Cultivo de antebrazo de rata
Consiguen cultivar un antebrazo de rata a partir de células de tal modo que, en teoría, no presente problemas de rechazo al implantarse.
|
Hay muchas ideas y estilos en las películas de ciencia ficción, incluso si sólo consideramos uno de los aspectos tratados en ellas.
Así por ejemplo, podemos fijarnos en que cuando en Star Wars a Luke Skywalker su padre le apunta una mano con un sable láser. La mano es reemplazada por un sistema biónico. Esta idea de implantar un brazo biónico a los que han sufrido algún tipo de accidente se viene investigando desde hace mucho tiempo con éxito desigual.
Otra posibilidad es crear órganos biológicos en el laboratorio, como ocurre en la película Blade Runner. Cualquier persona con cierta formación que viera esta película en esa época diría que la idea es absurda, pues, en teoría, no se pueden crear órganos sueltos, sino que se crean todos a la vez durante el desarrollo embrionario. Si no hay restricciones éticas y legales podemos crear un replicante que sea en realidad un ser humano modificado genéticamente para tener ciertas características, pero no crear un replicante a base de órganos que vamos uniendo unos a otros.
Sin embargo, un reciente logro nos permite vislumbrar un día en el que a un amputado se le implante un brazo orgánico que funcione como el que tenía y que encima no presente rechazo.
La foto que el amable lector puede ver encima de este texto es justamente una pata de rata que ha sido cultivada en laboratorio, no una pata de rata amputada sin más. Recordemos que las diferencias biológicas entre ratas y humanas son muy pocas, por lo que es posible que esto se pueda hacer con humanos a medio plazo.
Según Harald Ott ( Hospital General de Massachusetts en Boston), aunque, de momento, se han centrado en el cultivo de manos y antebrazo, la técnica se podría usar para obtener extremidades completas en general.
El desafío es que el miembro conseguido sea completamente funcional y esto no parece sencillo.
Aunque muchos amputados reciben un miembro artificial, su función suele ser meramente cosmética y no son funcionales. Cuando se trata de miembros biónicos se tiene cierta funcionalidad, pero los movimientos son muy artificiales y no se tiene un feedback sensorial. Y cuando se implanta una mano, por ejemplo de un donante muerto, el receptor tiene que recibir inmunodepresores de por vida para evitar el rechazo.
Un miembro biológico cultivado en laboratorio a partir de células del amputado puede solucionar todos estos problemas.
La técnica para cultivar este miembro de rata se ha usado previamente para cultivar corazones, pulmones y riñones. Incluso se ha usado ya, con un éxito variado, tejido cultivado de este modo para recrear faringes humanas.
En esta técnica se toma en primer lugar una muestra del órgano que se quiere regenerar de un donante y se trata con detergentes para separar las células del tejido blando. Lo que queda es un andamiaje de colágeno. Esto retiene la arquitectura del órgano original. En el caso del antebrazo de rata esto incluye la estructura de colágeno que soporta los vasos sanguíneos, los tendones, los músculos y los huesos.
En el segundo paso se toman células apropiadas del receptor y se siembra ese andamiaje para que las células lo colonicen en un biorreactor que proporciona nutrientes. Al final se obtiene un nuevo antebrazo que es compatible con el receptor del mismo y que no presentará problemas de rechazo con el sistema inmunitario.
Este caso del antebrazo de rata ha sido mucho más complicado de realizar que los casos anteriores, pues fue necesario suspender el antebrazo en crecimiento de turno y proporcionar riego sanguíneo con nutrientes y oxígeno a su sistema circulatorio. Además, fue necesaria la estimulación eléctrica para saber si era funcional.
Esto implicó empezar con la introducción de células epiteliales en las superficies de las venas y arterias para que estas formaran unos vasos más naturales que fueran más resistentes que el simple colágeno.
Los investigadores introdujeron después una mezcla de células que incluían mioblastomas en las cavidades destinadas a los músculos, células que dieron lugar a esos mismos músculos. También se regeneraron las células de los huesos.
En un plazo de dos a tres semanas el antebrazo de rata había sido reconstruido. La tasa de éxito no es baja, pues este grupo de investigación consiguió recelularizar 50 de los 100 miembros descelularizados.
La cuestión era saber si el miembro podría llegar a ser funcional o no. Así que usaron estímulos eléctricos para activarlo. Pudieron ver que se podía conseguir flexionar los distintos músculos. A partir este éxito decidieron implantar el antebrazo así conseguido a una rata. Comprobaron que la sangre circulaba por el nuevo miembro sin problema, pero no comprobaron si había movimiento en el nuevo miembro o si este sufría rechazo.
Les falta por demostrar que se desarrolla correctamente un sistema nervioso. En personas a las que se les ha transplantado una mano, los nervios del receptor crecen en la mano donante para tomar control del nuevo miembro. Todavía no está claro que esto suceda igualmente en este caso.
El grupo de Ott quiere hacer lo mismo con antebrazos de primates y de momento ya han conseguido descelularizarlos con éxito. También ya han empezado a recelularizarlos con células humanas, al menos el primer paso relativo a los vasos sanguíneos.
Sólo en los EEUU hay 1,5 millones de amputados para los que este tipo de técnica podría ser crucial. Pero, obviamente, se necesitará mucho esfuerzo y años de investigación hasta que esto se pueda usar en humanos con ciertas garantías.
Entre los desafíos está que incluso los pequeños capilares se recelularicen bien y que no haya problemas de coágulos o colapsos. Otro problema es que la mano en particular contiene una red muy compleja de nervios que deben funcionar a la perfección para que la mano sea funcional, de otro modo sólo sería una mano cosmética, aunque biológica.
Si la técnica finalmente funciona habrá que extender la política de donaciones para incluir brazos y piernas. Al fin y al cabo, también se necesita un donante en este caso. Pero, ¿será posible imprimir ese andamiaje de colágeno con una impresora 3D en un futuro no tan lejano?
Copyleft: atribuir con enlace a http://neofronteras.com/?p=4691
Fuentes y referencias:
Artículo original
Foto: Image: B J Jank, Ott Laboratory
4 Comentarios
RSS feed for comments on this post.
Lo sentimos, esta noticia está ya cerrada a comentarios.




lunes 8 junio, 2015 @ 8:54 pm
– Estos avances son realmente sorprendentes,e incluso esperanzadores, de una complejidad extraordinaria. Es por ello que a la pregunta de si es posible reproducir ese andamiaje de colágeno con una impresora 3D,dudaría mucho en responder afirmativamente,aunque no digo que en un futuro con una tecnología y unos conocimientos más precisos fuera ello posible. Tengo presente que ya se diseñó con una impresora 3D, una hamburguesa de auténticas células.
jueves 11 junio, 2015 @ 3:43 pm
Tal vez estén puesta ahí las esperanzas en el ojo biónico, que permita recuperar la visión a las personas ciegas, mas que en un aparato que les permita ver, como la que salia en Estar Treek New Generación. Uno de la nueva tripulación, llevaba una especie de gafas videocámaras, con la que podía ver el mundonbexterior, llevándolas siempre puestas.
También he leído, que ya están haciendo pruebas con células madres, para que regeneren el páncreas o mas bien, creen uno artificial, que suministre insulina a diabéticos, y estos, no tengan que ponerse inyecciones de insulina, ni tener que tomar metformina, ni tener que realizar controles de glucemia.
Y si pueden repararse cortes en extremidades graves en un futuro, fantástico. Se acabara eso de llevar prótesis de plástico.
?También servirá para construir robots orgánicos, mas parecido a nosotros, o a animales ya extintos, como los que salen en Parque Jurasico, talla reducida, con gran reaLismo.?
viernes 12 junio, 2015 @ 9:04 pm
En efecto, el artículo es de los que asombran. Añado a lo que dicen mis compañeros: ¿puede también ser posible un corazón que, inicialmente, funcione junto al deteriorado y lo sustituya definitivamente cuando éste se extirpe por el peligro que pueda representar mantenerlo? En ese caso los corazones artificiales acabarían siendo cosa superada.
Bueno; es un especular…
viernes 19 junio, 2015 @ 5:46 pm
Aún falta ver si el brazo se mueve y acaba funcionando correctamente. Por lo demás, un resultado muy prometedor.
Sobre lo que comentas, amigo David, son cosas que ya están en el horizonte más próximo, excepto los robots orgánicos que habría que colocarlos en un futuro más distante.